新闻来源:鼻咽癌防治中心
7月21日,中山五院副院长、鼻咽癌防治中心首席专家陈明远教授团队在国际权威期刊《自然遗传学》(Nature Genetics)上发表了文章“Single-cell and spatial transcriptomics reveal mechanisms of radioresistance and immune escape in recurrent nasopharyngeal carcinoma”。该研究系统阐明了复发鼻咽癌中特异性肿瘤微环境介导放疗抵抗与免疫逃逸发生机制,并创新性提出靶向免疫微环境逆转放疗抵抗和免疫逃逸的精准策略,为治愈复发鼻咽癌提供重要的理论基础。
二程放疗是局限期复发鼻咽癌重要的根治手段。然而,常规二程放疗毒性大,约25%的患者会出现致死性的毒性反应。研究团队前期提出的分次低剂量“超分割”放疗模式,显著降低了致死性并发症发生率17.0%,将患者3年总生存率从55.0%提升到74.6%。相关研究成果被美国NCCN治疗指南采纳,成为复发鼻咽癌标准治疗手段。然而,约30%接受超分割放疗的患者会出现局部复发,且95%的复发病灶位于放疗高剂量区。这些临床现象提示放疗抵抗是鼻咽癌局部复发的关键原因。
2023年2月国际著名医学期刊《柳叶刀》发表
针对广泛期复发鼻咽癌,药物治疗是其唯一的挽救治疗手段。研究团队前期提出化疗+抗血管生成治疗+免疫治疗(创新“化靶免”联合方案);接受该方案治疗的患者中位无进展生存期(mPFS)为25.8个月,高于既往“化免”方案(mPFS:9.6月)。≥3级治疗相关的毒性发生率为56.1%,低于“化免”标准方案的87%。然而,患者在后续的免疫治疗维持期间,均会因为免疫治疗耐药导致治疗失败。肿瘤微环境介导的免疫逃逸机制将影响免疫治疗的疗效。
2023年2月国际权威肿瘤学期刊《临床肿瘤学杂志》发表
2022年10月Cell旗下医学旗舰刊 《Med》发表
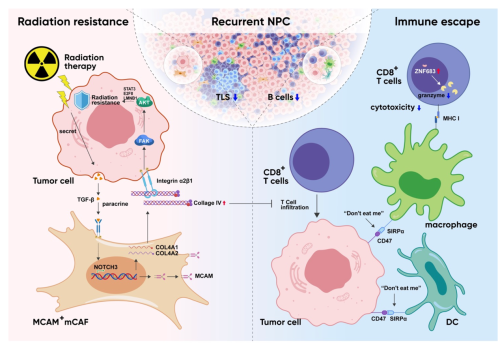
基于上述研究背景,研究团队对24例患者的39个初治-复发配对组织样本行单细胞测序与空间转录组测序,解析初治-复发鼻咽癌肿瘤微环境差异。研究团队鉴定了与复发鼻咽癌放疗抵抗显著相关的肿瘤相关成纤维细胞亚群:MCAM+ 肌成纤维细胞(MCAM+ myCAFs)。分子机制研究发现,MCAM+ myCAFs通过分泌IV型胶原与肿瘤细胞表面ITGA2结合并激活FAK-PI3K-AKT信号轴,进一步,调控DNA损伤修复的核内特异转录因子,增强肿瘤细胞辐射抵抗。此外,IV型胶原能显著抑制T细胞浸润,导致肿瘤细胞免疫逃逸发生。相反,肿瘤细胞在接受辐照后,会释放大量炎症因子TGF-β,诱导并维持MCAM+ myCAFs的表型和功能维持。研究团队还进一步发现复发鼻咽癌肿瘤微环境中介导的特异免疫逃逸机制:1.一类细胞毒功能受损的组织驻留型T细胞(ZNF683+ CD8+T)显著富集;2.B细胞及三级淋巴结结构显著降低;3.肿瘤细胞与髓系细胞空间距离更近且广泛存在CD47-SIRPa相互作用。
研究机制图
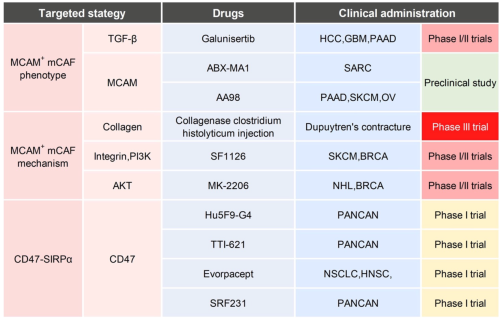
根据这些发现,研究团队提出靶向肿瘤微环境逆转放疗抵抗和免疫逃逸的治疗策略。例如,采用TGF-β抑制剂Galunisertib或AKT抑制剂MK2206联合超分割放疗,在超分割放疗“减毒”的基础上,联合精准靶向治疗,逆转放疗抵抗,有望进一步提高复发鼻咽癌二程放疗的疗效。此外,在免疫治疗失败的复发患者中,采用CD47抗体Evorpacept,有望逆转免疫逃逸,进一步提高全身药物治疗疗效。相关临床试验正在进行中。
临床转化靶点
陈明远教授、张世华教授、夏天亮副研究员、刘友平副主任医师、游瑞副主任医师为本文的共同通讯作者;游瑞副主任医师,沈群伦博士,林超博士,董康宁博士,刘晓研究生与徐寒石技术员为本文共同第一作者。
审稿专家:陈明远
通讯员:游瑞